MAP-Xing der Malaria-Proteinkomplexe
Ein internationales Forschungsteam unter der Leitung des Bozdech-Labors an der Nanyang Technical University in Singapur und des Gilberger-Labors am Zentrum für Strukturelle Systembiologie und am Bernhard-Nocht-Institut für Tropenmedizin in Deutschland enthüllt die globale Landschaft der Protein-Protein-Interaktionen, die die Biologie des Malariaparasiten bestimmen. Ihr neuer Ansatz namens „Meltome-assisted profiling of protein complexes” (MAP-X) wurde kürzlich in Nature Microbiology veröffentlicht.
Mit über einer halben Million Todesfällen pro Jahr bleibt Malaria eine große Belastung für die globale Gesundheit. Die tödlichste Form der Malaria wird durch den Parasiten Plasmodium falciparum verursacht. Es wurden erhebliche Anstrengungen unternommen, um Malariamedikamente zu entwickeln und einzusetzen, was zu einem Rückgang der Todesfälle geführt hat. Leider werden diese Fortschritte durch das Auftreten resistenter Parasiten gefährdet. Die Entwicklung neuartiger Therapeutika erfordert ein besseres Verständnis der Zell- und Molekularbiologie des Parasiten selbst.
Plasmodium falciparum besteht aus über 5.200 verschiedenen Proteinen und ist während seines komplexen Lebenszyklus auf ein dynamisches Netzwerk von Protein-Protein-Wechselwirkungen angewiesen.
„Um die molekularen Mechanismen zu verstehen, die die komplexe Biologie des Parasiten steuern, ist es wichtig, nicht nur die Rolle jedes einzelnen Proteins zu verstehen, sondern auch deren Wechselwirkungen untereinander“, sagt Tim Gilberger, Leiter der Abteilung Zelluläre Parasitologie am BNITM. „Allerdings sind die Funktion und die molekularen Wechselwirkungen von über 40 Prozent der Proteine von Plasmodium falciparum derzeit noch unbekannt, ganz zu schweigen von dem unerforschten Gebiet ihrer dynamischen Wechselwirkungen und Komplexbildung während der Parasitenvermehrung.“
Um neue Proteininteraktionen zu entdecken, verwendeten die Forscher eine hochmoderne Methode, die als thermisches Proteom-Profiling (TPP) bekannt ist.

„TTP untersucht die thermische Stabilität von Proteinen in intakten Zellen“, erklärt Samuel Pazicky, der Erstautor der Studie. „Wenn sie Hitze ausgesetzt werden, werden Proteine, die miteinander interagieren, auf ähnliche Weise zerstört.“
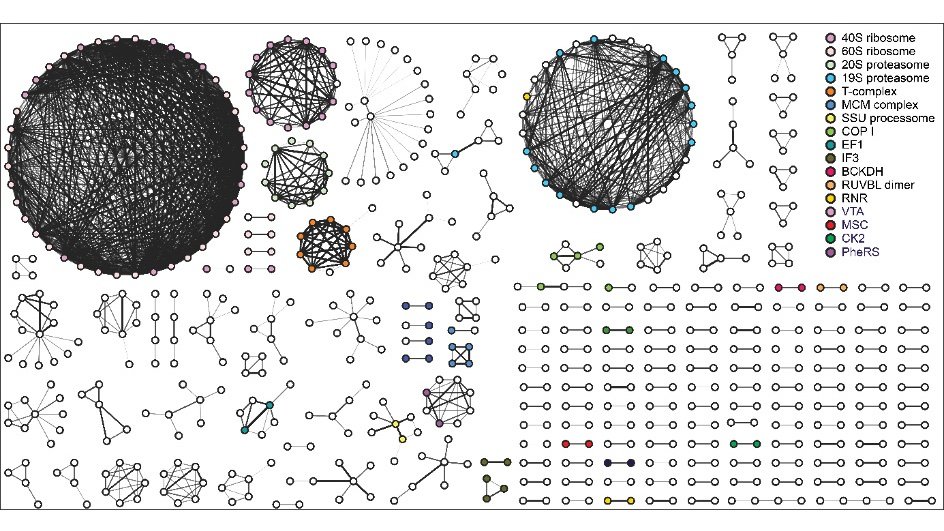
Das Forschungsteam kombinierte dann TPP mit künstlicher Intelligenz, um die Protein-Protein-Interaktionen zu kartieren und vorherzusagen. Dieser neue Ansatz, der als „meltome-assisted profiling of protein complexes“ (MAP-X) bezeichnet wird, wendet maschinelles Lernen auf TPP-Daten an, um Tausende von Proteinen zu überwachen und zu vergleichen, während sie in Zellen exprimiert werden. „Wir haben MAP-X auf sieben Zeitpunkte im Lebenszyklus von Plasmodium falciparum im menschlichen Blut angewendet und dabei mehr als 20.000 Interaktionen entdeckt“, erklärt Pazicky.
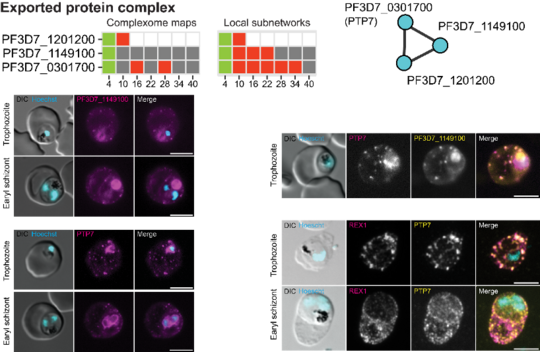
Mit MAP-X bestätigte das Team nicht nur die Existenz bekannter Proteinkomplexe, sondern entdeckte auch Blaupausen für neuartige parasitenspezifische Proteinkomplexe und biochemische Signalwege. „Die von MAP-X erstellten Interaktionskarten konnten bisher unbekannte Proteinkomplexe vorhersagen“, sagt Zbynek Bozdech, der korrespondierende Autor der Veröffentlichung. „Die Existenz mehrerer dieser Komplexe wurde durch Fluoreszenzmikroskopie und Pull-down-Assays experimentell weiter verifiziert.“
„Mit seiner Fähigkeit, bisher unbeschriebene Interaktionen zu identifizieren und stadiumspezifische Dynamiken aufzudecken, ist MAP-X eine leistungsstarke Ressource, um die dynamischen Interaktionen und grundlegenden biologischen Prozesse des Malariaparasiten zu entschlüsseln“, erklärt Gilberger. MAP-X soll dazu beitragen, die Entwicklung von Malariamedikamenten der nächsten Generation zu steuern, da bestehende Behandlungen zunehmend durch Resistenzen bedroht sind. Außerhalb der Malariaforschung stellt MAP-X eine neue Methode dar, Proteinkomplexe in jeder Art von Zelle zu kartieren, einschließlich Bakterien, anderer Parasiten sowie Blut, Pflanzen oder Geweben.
Originalpublikation
Pazicky S. et al.: MAP-X reveals distinct protein complex dynamics across Plasmodium falciparum blood stages. Nat Microbiol. (28 Nov. 2025). doi.org/10.1038/s41564-025-02173-7
Ansprechperson
Prof. Dr. Tim-Wolf Gilberger
Abteilung Zelluläre Parasitologie
Telefon : +49 40 8998 87600
E-Mail : gilberger@bnitm.de
Melissa Prass
Presse- und Öffentlichkeitsarbeit CSSB
Telefon : +49 40 8998-87502
E-Mail : melissa.prass@cssb-hamburg.de
Julia Rauner
Presse- & Öffentlichkeitsarbeit
Telefon : +49 40 285380-264
E-Mail : presse@bnitm.de
Weiterführende Informationen






