Entscheidender Aktivator der angeborenen Immunabwehr gegen Darmparasiten entdeckt
Parasitäre Wurminfektionen stellen mit über 1,6 Milliarden Betroffenen eine der größten Herausforderungen der globalen Gesundheit dar. Forschende des Bernhard-Nocht-Instituts für Tropenmedizin (BNITM) haben nun einen entscheidenden Mechanismus bei der Abwehr von Wurmparasiten entdeckt. Im Zentrum steht ein Molekül namens CD160, das auf bestimmten Immunzellen vorkommt. Die Studie zeigt erstmals, dass dieses Molekül eine Schlüsselrolle dabei spielt, wie effektiv der Körper Darmwürmer bekämpfen kann. Die Studienergebnisse erschienen kürzlich in der Fachzeitschrift Mucosal Immunology.
Schätzungen zufolge kommt weltweit ein Viertel der Bevölkerung im Laufe des Lebens mit parasitären Würmern in Kontakt, insbesondere in tropischen Regionen. Obwohl man weiß, dass der Körper solche Infektionen vor allem über eine sogenannte Typ-2-Immunantwort bekämpft, sind die genauen Abläufe dabei noch nicht vollständig verstanden. Forschende des BNITM nutzten in der nun veröffentlichten Studie den Fadenwurm Strongyloides ratti (S. ratti) als Modell, um diese Prozesse genauer zu untersuchen. Sie infizierten Mäuse mit dem Fadenwurm.
Die infektiösen Larven von S. ratti leben in der feuchten Erde und dringen zunächst durch die Haut in den Körper ein, wandern durch Gewebe bis in den Kopfbereich, werden dann geschluckt und entwickeln sich im Dünndarm zu erwachsenen Würmern. Diese legen Eier, welche mit dem Stuhl ausgeschieden werden und sich wieder zu infektiösen Larven entwickeln. Um die Würmer aus dem Körper zu eliminieren, werden verschiedene Immunzellen aktiv: Unter anderem reagieren Immunzellen des angeborenen Immunsystems, die „group 2 innate lymphoid cells“ (ILC2), schnell und aktivieren über Botenstoffe Mastzellen. Diese übernehmen im Darm eine zentrale Rolle in der Abwehr der Würmer.
Das Checkpoint-Molekül CD160 im Fokus
CD160 ist ein kleines Checkpoint-Molekül auf der Oberfläche bestimmter Immunzellen, das wie ein Kontrollschalter funktioniert.
„Solche Checkpoint-Moleküle helfen dem Immunsystem dabei, seine Aktivität genau zu steuern. Das ist wichtig, damit es Krankheitserreger wirksam bekämpft, ohne den eigenen Körper zu schädigen“, erklärt Dr. Lennart Heepmann, Erstautor der Publikation und Postdoc in der Arbeitsgruppe Helminthen-Immunologie am BNITM. „Wir haben nun erstmals gezeigt, dass CD160 auf den ILC2 im Darm der Maus vorkommt.“

Die Forschenden konnten zudem zeigen, dass sich die ILC2 während einer Infektion mit S. ratti in zwei funktionell unterschiedliche Gruppen aufteilen. Eine Gruppe trägt das Molekül CD160 auf ihrer Oberfläche. Diese Zellen vermehren sich stark, produzieren aber nur wenige Botenstoffe. Die zweite Gruppe besteht aus ILC2 ohne CD160. Diese produzieren große Mengen wichtiger Typ-2-Botenstoffe, welche die Mastzellen aktivieren und so die Abstoßung der Würmer im Darm auszulösen. Entscheidend ist dabei, dass sich die CD160-positiven ILC2 im Verlauf der Immunreaktion in CD160-negative, botenstoffproduzierende ILC2 umwandeln können.
CD160 ist entscheidend für die Eliminierung des Parasiten
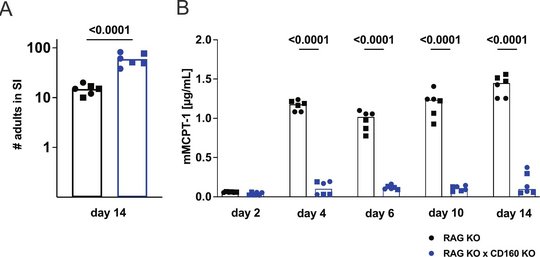
Deutlich wurde die Bedeutung von CD160 in Experimenten mit Mäusen, die so genetisch verändert wurden, dass ihnen das CD160-Molekül fehlte (CD160-Knockout Mäuse): Sie konnten die Parasiten im Darm nicht wirksam bekämpfen. Die Infektion hielt ungewöhnlich lange an und die Parasiten blieben über Wochen und Monate im Körper, bis zu etwa 100 Tage. Mäuse hingegen, die das CD160-Molekül besaßen, reagierten deutlich effektiver: Ihr Immunsystem konnte die Parasiten innerhalb weniger Tage stark reduzieren. Der Grund für die lange Infektion in den CD160-Knockout Mäusen: Die wichtigen Mastzellen wurden nicht aktiviert, weil die nötigen Signale der ILC2 ausblieben. Die Forschenden schlossen aus ihren Experimenten, dass sich CD160-positive ILC2 zunächst stark vermehren und sich anschließend in botenstoffproduzierende ILC2 ohne CD160 entwickeln. Die Botenstoffe dieser CD160-negativen ILC2 aktivieren die Mastzellen, die letztlich dafür sorgen, dass die Parasiten aus dem Darm ausgeschieden werden.

„Das hat uns wirklich überrascht“, sagt Studien- und Arbeitsgruppenleiterin Prof. Minka Breloer. „CD160 war bisher vor allem als regulierendes Molekül auf anderen Immunzellen, zum Beispiel auf natürlichen Killerzellen oder T-Zellen, bekannt. Anders als viele andere Checkpoint-Moleküle, die Immunreaktionen eher bremsen, fördert CD160 in unseren Experimenten die Vermehrung und Entwicklung wichtiger Abwehrzellen. Das eröffnet eine völlig neue Perspektive auf die Steuerung der Immunantwort.“
Die Forschenden zeigten auch, dass das Fehlen von CD160 in den CD160-Knockout Mäusen direkt ursächlich für die lange Infektionsdauer mit S. ratti war: Wenn sie bereits infizierte CD160-Knockout Mäuse mit CD160-positive ILC2 behandelten, ließ sich der Immundefekt teilweise beheben. Die Mastzellen waren wieder aktiv und die Anzahl der Parasiten sank.
Neue Therapieoptionen bei anderen Erkrankungen
Die Ergebnisse liefern nicht nur ein neues Verständnis darüber, wie das Immunsystem Wurminfektionen bekämpft. Sie zeigen auch, dass sich Immunzellen dynamisch entwickeln und ihre Funktion im Verlauf einer Infektion verändern. Die Entdeckung der CD160-positiven ILC2 könnte langfristig neue Ansätze für Therapien eröffnen, etwa bei Parasiteninfektionen, aber auch bei Allergien wie Asthma oder anderen entzündlichen Erkrankungen, bei denen die Typ-2-Immunantwort eine Rolle spielt.
„Wir sehen hier einen grundlegenden Mechanismus, der weit über diese spezielle Infektion mit S. ratti hinaus relevant sein könnte“, sagt Heepmann. „Das macht die Entdeckung so spannend. Die Ergebnisse liefern auch Ansatzpunkte für zukünftige Immuntherapien, zum Beispiel in der Krebsbehandlung. Über Checkpoint-Moleküle können wir gezielt in die Steuerung von Immunzellen eingreifen, um Abwehrreaktionen je nach Erkrankung zu verstärken oder zu dämpfen.“
Immunologischer Hintergrund
Das angeborene Immunsystem ist der Teil der Immunabwehr, der sofort auf Eindringlinge reagiert, ohne sie zuvor „kennenlernen“ zu müssen. Es erkennt allgemeine Gefahrensignale und setzt schnell erste Schutzmechanismen in Gang. Wurminfektionen werden im Rahmen von der sogenannten Typ-2-Immunantwort bekämpft. In diesem Prozess spielen ILC2 (= „group 2 innate lymphoid cells“) eine zentrale Rolle: Sie nehmen Warnsignale aus dem Gewebe wahr, werden dadurch aktiviert, vermehren sich und geben die Warnsignale in Form von Botenstoffen wie IL-5 (= Interleukin-5), IL-13 und IL-9 weiter. Dadurch aktivieren sie weitere Immunzellen, unter anderem Mastzellen im Darm, die schließlich dafür sorgen, dass die Parasiten aus dem Körper ausgeschieden werden. Diese frühe Reaktion kann die Parasiten bereits deutlich eindämmen, doch für eine vollständige Eliminierung ist zusätzlich das adaptive, also das erlernte Immunsystem notwendig. Dazu gehören zum Beispiel T-Zellen und B-Zellen, die gezielt gegen Krankheitserreger vorgehen und eine länger anhaltende Immunität aufbauen. Für die Studie nutzten die Forschenden sogenannte RAG-Knockout-Mäuse. Diese Tiere besitzen kein funktionierendes adaptives Immunsystem, also keine T- und B-Zellen. So konnten die Forschenden gezielt die angeborene Immunabwehr allein untersuchen. Die Studie zeigt, wie entscheidend die Steuerung der frühen Phase der Immunantwort für den weiteren Verlauf der Infektion ist.
Publikation
Heepmann L. et al., CD160-competent ILC2 are crucial for the ejection of intestinal helminths by the innate immune system, Mucosal Immunology 2026, DOI: 10.1016/j.mucimm.2026.04.005
Die Deutsche Forschungsgemeinschaft (DFG) und die Joachim Herz Stiftung haben die Studie finanziell unterstützt.
Ansprechperson
Dr. Lennart Heepmann
Arbeitsgruppe Helminthen-Immunologie
Telefon : +49 40-285380 -860 -863
E-Mail : lennart.heepmann@bnitm.de
Prof. Dr. Minka Breloer
Leiterin Arbeitsgruppe Helminthen-Immunologie
Telefon : +49 40 285380-830
Fax : +49 40 285380-400
E-Mail : breloer@bnitm.de
Dr. Anna Hein
Presse- & Öffentlichkeitsarbeit
Telefon : +49 40 285380-269
E-Mail : presse@bnitm.de
Weiterführende Informationen






